技术支持Technical Support
联系我们CONTACT US
 400 179 0116
400 179 0116
24小时服务热线
划重点-细胞敲除必备
来源:启达生物 浏览量:2694 发布时间:2023-04-27
走上人迹罕至的道路,产生一个敲除细胞系而不是敲除细胞?我们在这篇文章中为您介绍了利用同源定向修复途径、设计最佳供体DNA以及避免此类基因组编辑中常见事故的技巧和窍门。
敲入突变和基因编辑
靶向基因组编辑事件分为两大类:细胞敲除和动物敲除。敲除的目的是通过产生移码突变来破坏DNA翻译。大多数细胞修复事件都会产生这些类型的突变,使其成为一项“简单”的编辑工作。然而,对于敲门砖来说,情况并非如此。敲入突变通常需要在精确的基因组位置结合精确的DNA序列,几乎没有错误的余地。毫不奇怪,这些编辑比淘汰对手需要更多的计划和技巧。
要开始一个敲门实验,首先要问的问题是从哪里敲除,所以需要确定你想在基因组中引入你的敲门砖的位置。然后再选择使用哪种Cas酶,并设计一个gRNA到你想引入编辑的地方。最后,你必须知道引入什么序列,这是通过设计和使用供体DNA分子来完成的。你的供体分子需要与新序列两侧的靶基因座具有同源性。这种同源性将引导细胞使用供体DNA作为修复的模板,这样才会让你的序列的结合,最后敲除成功!那么,捐赠者是如何被用作修复的模板的呢?请看以下分解。
同源性定向修复与基因组工程
制造敲除细胞系的最简单方法是利用细胞已经具有的内置修复途径来修复DNA双链断裂——(HR)。
HR是哺乳动物细胞中占主导地位的同源定向修复(HDR)途径,但通常是一种不太常见的DNA修复机制。平均而言,它只占DNA修复不到10%,不同细胞类型的修复率各不相同。差异可能是由细胞周期速率引起的;快速生长的细胞将比缓慢的细胞具有更高的HR频率。重要的是要知道HR经常在癌症细胞中发生突变,特别是在实验室常用的乳腺和卵巢细胞系中。建议您在尝试HDR敲除之前检查细胞系中HR相关的突变。
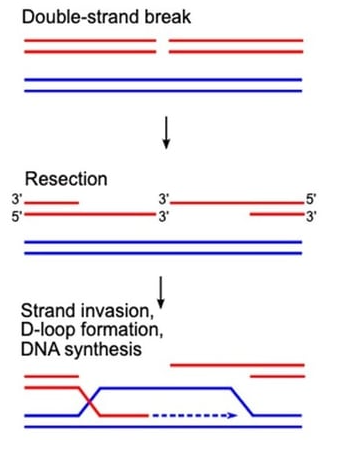
图1:通过同源重组修复DNA双链断裂的早期步骤。
设计HDR
HDR途径的基础依赖于模板分子的修复,模板分子通常是内源性可用的姐妹染色单体,尽管也可以使用外源DNA。以下是为成功的HDR活动设计供体DNA的一些考虑因素。
CRISPR切割位置
将CRISPR切割部位尽可能靠近敲入位置。HDR依赖于在断裂部位切除形成ssDNA,并利用ssDNA的末端找到修复模板。当插入物在断裂的10bps以内时,观察到最高的HDR效率,使切割基本上作为模板DNA的一部分。
同源序列和样本类型
为了确保你的供体分子被用作模板,你需要在敲入位点的右边和/或左边加入同源序列。该序列的长度和组成(单股与双股)都取决于载体的大小。同源序列至40bps的单链寡核苷酸供体(ssODN)可以有效地敲入几百bps的序列。然而,如果你有一个更大的敲除(200 bp–2 kb),由于寡核苷酸的合成限制,将需要使用dsDNA供体。这些载体传统上在500bp至1kb范围内具有较大的同源序列,然而,最近也有使用了较短的同源区并取得了一些成功(Yu等人,Nat Chem Biol)。
突变PAM或sgRNA序列
Cas9可能在靶位点经历多轮切割,直到PAM位点或引导物识别序列的一部分通过突变被破坏。通过在供体DNA的PAM或引导识别序列中引入突变,可以保证HDR后不会再靶向。如果你的Cas9切入了一个基因的编码区,请确保你引入的PAM编辑是一个沉默的突变,这样你就不会意外地改变你感兴趣的蛋白质。
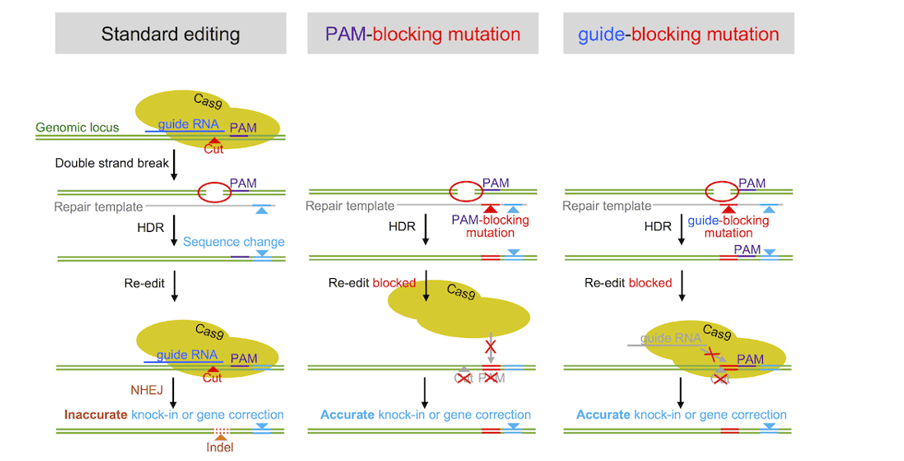
图2:停止PAM的再切割并引导供体DNA中RNA破坏突变
将HDR提升到其他编辑之上
HDR并不是DNA修复最常见的编辑途径。在HDR编辑时要倾斜刻度,您可以尝试以下一个或多个不同的编辑位置。
其他修复机制
除了HR之外,哺乳动物细胞还有两种主要的修复机制——非同源末端连接(NHEJ)和替代末端连接(alt-EJ)。对这两种途径的重要成分的抑制剂已被证明对增加HR编辑成功是有效的(Yang等人,Int J Mol Sci)。在引入Cas9之前和之后,将这些抑制剂添加到培养基中会增加HDR,只需确保在一两天内去除抑制剂,以免影响细胞的生存能力。
富集S期细胞
HR主要作用于细胞周期的S期和G2期,此时姐妹染色单体可能作为修复模板存在。要最大限度地提高HDR释放,请确保细胞在细胞周期阶段中积极循环。如果细胞过度融合或培养基中没有足够的营养物质,它们就不会进行DNA复制,所以一定要注意这些细胞!更进一步,你可以抑制负责S期过渡的细胞周期调节蛋白,使细胞在HDR促进的周期中停留更长时间。如果细胞停留时间过长,这种方法可能会对生存能力产生一些负面影响。长时间的细胞周期停滞可以在短短10小时内导致细胞凋亡。
使用快速的Cas剪辑
如果晋升人力资源就像换掉你的Cas9一样简单呢?可以!Cas12a是Cas家族成员,在切割时会产生粘性末端。Cas12a可能通过在断裂部位产生ssDNA悬突来促进HDR,这是早期的HR步骤(Moreno-Mateos等人,Nat-Com)。
另一种用于启动HR的Cas断裂的方法是将HR蛋白融合到核酸酶上。与Cas9融合的早期HR因子已被证明可以通过在其他因子加载到断裂上之前中断进行HR来增加HDR频率,从而可能使修复沿着不同的途径来进行(Charpentier等人,Nat-Com)。
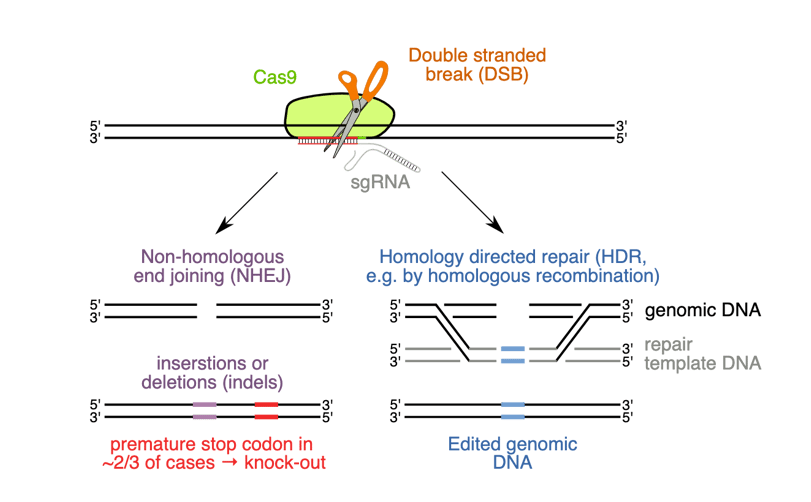
图3:HDR切入与NHEJ介导的小插入和缺失型编辑竞争。
References
Yu, Y., Guo, Y., Tian, Qigi, Lan, Y., et. al. An efficient gene knock-in strategy using 5’-modified dsDNA donors with short homology arms. Nat Chem Biol., 308(20): 1-9 (2020). 10.1038/s41589-019-0432-1
Mehdi Banan. Recent advances in CRISPR/Cas9-mediated knock-ins in mammalian cells. J Biotechnol., 16(4): 387-390 (2020). 10.1016/j.jbiotec.2019.11.010
Wright, D. W., Shah, S. S., Heyer, W. D. Homologous recombination and the repair of DNA double strand breaks. J Biol Chem., 293(27): 10524-10535 (2018). 1 10.1074/jbc.TM118.000372
Yang, H., Ren, S., Yu, S., Pan, H., et al. Methods favoring homology-directed repair choice in response to CRISPR/Cas9 Induced-double strand breaks. Int J Mol Sci., 21(18): 6461 (2020). 10.3390/ijms21186461
Lin, S., Staahl, B. T., Alla, R. K., Doudna, J. A. Enhanced homology-directed human genome engineering by controlled timing of CRISPR/Cas9 delivery. eLIFE. (2014) 10.7554/eLife.04766
Moreno-Mateos, M. A., Fernandez, J. P., Rouet, R., Vejnar, C. E., et al. CRISPR-Cpf1 mediates efficient homology-directed repair and termperature-controlled genome editing. Nat. Com., 8(2024), (2017). 10.1038/s41467-017-01836-2
Charpentier, M., Khedher, A. H. Y., Menerot, S., Brion, A., et al. CtIP fusion to Cas9 enhances transgene integration by homology-dependent repair. Nat. Com., 9-1133 (2018). 10.3390/ijms21186461







